Мезенхимальные дистрофии (стромально-сосудистые).
- Подробности
Мезенхимальные дистрофии развиваются в результате нарушений обмена в соединительной ткани и выявляются в строе органов и стенках сосудов. При нарушениях обмена в соединительной ткани, преимущественно, в ее межклеточном веществе, накапливаются продукты метаболизма, которые могут приноситься с кровью и лимфой, быть результатом извращенного синтеза или появляться в результате дезорганизации основного вещества и волокон соединительной ткани.
1. Стромально-сосудистые диспротеинозы
С дистрофиям такого типа относят мукоидное набухание, фибриноидное набухание, гиалиноз, амилоидоз.
Нередко мукоидное набухание, фибриноидное набухание и гиалиноз являются последовательными стадиями дезорганизации соединительной ткани. В основе этого процесса лежат накопление продуктов плазмы крови в основном веществе в результате повышения тканево-сосудистой проницаемости (плазморрагия), деструкция элементов соединительной ткани и образование белково-полисахаридных комплексов. Амилоидоз отличается тем, что в состав образующихся комплексом входит аномальный белок, который синтезируют амилоидобласты.
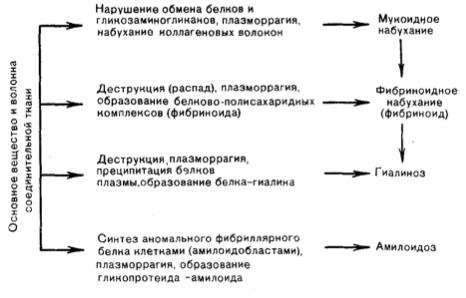
1) Мукоидное набухание
Поверхностная и обратимая дезорганизация соединительной ткани. При этом в основном веществе происходят накопление и перераспределение гликозаминогликанов за счет увеличения содержания прежде всего глюкуроновой кислоты. Так как гликозаминогликаны обладают повышенными гидрофильными свойствами, их накопление обуславливает повышение тканевой и сосудистой проницаемости. В результате к ГАГ примешиваются белки плазмы (в основном, глобулины) и гликопротеиды. Развиваются гидратация и набухание основного межуточного вещества.
Микроскопия: основное вещество базофильное. Возникает феномен метахромазии – изменение состояния основного межуточного вещества из-за изменения рН с накоплением хромотропных веществ. Коллагеновые волокна набухают, обычно сохраняют пучковое строение. Становятся малоустойчивыми к действию коллагеназы.
Изменения могут сопровождаться появлением лимфоцитарных, плазмоклеточных и гистиоцитарных инфильтратов.
Такой тип набухания встречается в различных органах и тканях, но чаще в стенках артерий, клапанах сердца, эндокарде, эпикарде, то есть там, где хромотропные вещества встречаются и в норме (однако при патологии их количество резко возрастает).
Внешний вид: ткань или орган сохранены.
Причины: гипоксия, инфекционные и аллергические заболевания, ревматические болезни, атеросклероз, эндокринопатия и т.д.
Исход: двоякий. Либо полное восстановление ткани, либо переход в фибриноидное набухание.
2) Фибриноидное набухание.
Глубока и необратимая дезорганизация соединительной ткани, в основе которой лежит деструкция ее основного вещества и волокон, сопровождающаяся резким повышением сосудистой проницаемости и образование фибриноида. Фибриноид – сложное вещество, в состав входят белки и полисахариды распадающихся коллагеновых волокон, основного вещества и плазмы крови, а также клеточные нуклеопротеиды. Обязательным компонентом является фибрин.
Микроскопия: пучки коллагеновых волокон, пропитанные плазмой, становятся гомогенными, образуя с фибрином нерастворимые прочные эозинофильные соединения. Метахромазия тканей не выражена или выражена слабо (так как ГАГ основного вещества деполимеризованы).
Внешний вид: внешне органы и ткани мало изменяются.
Причины: чаще всего это проявление инфекционно-аллергических, аутоиммунных и ангионевротических реакций. В таких случаях набухание носит системный характер. Местно фибриноидное набухание может возникать при воспалении, особенно, хроническом.
Исход: характеризируется развитием фибриноидного некроза, замещением очага деструкции соединительной тканью (склероз) или гиалинозом.
Такое набухание ведет к нарушению, иногда к прекращению функции органа.
3) Гиалиноз
В соединительной ткани образуются однородные полупрозрачные плотные массы, напоминающие гиалиновый хрящ. Ткань при этом уплотняется.
В развитии гиалиноза ведущую роль играют деструкция волокнистых структур и повышение тканево-сосудистой проницаемости. С плазморрагией связаны пропитывание ткани белками плазмы и адсорбция их на измененных волокнистых структурах с последующей преципитацией и образованием гиалина. В образовании сосудистого гиалина принимают участие гладкомышечные клетки. Гиалиноз может развиваться в исходе различных процессов: плазматического пропитывания, фибриноидного набухания, воспаления.
Различают:
А) гиалиноз сосудов
Гиалинозу подвергаются преимущественно мелкие артерии и артериолы. Ему предшествуют повреждения эндотелия, его мембраны и гладкомышечных клеток стенки и пропитывание ее плазмой крови.
Микроскопия: гиалин обнаруживается в субэндотелиальном пространстве6 он оттесняет кнаружи и разрушает эластическую пластинку, средняя оболочка истончается, в фиале артериолы превращаются в утолщенные стеклянные трубки с резко суженным или полностью закрытым просветом.
Такой гиалиноз носит системный характер, однако6 наиболее выражен в почках, головном мозге, сетчатке глаза, поджелудочной железе., коже. Характерен для гипертонической болезни, диабетической микроангиопатии и заболеваний с нарушениями иммунитета. Как физиологическое явление местный гиалиноз артерий наблюдается в селезенке взрослых и пожилых людей (отражает функционально-морфологические особенности этого органа – депонирование крови).
Сосудистый гиалин – вещество преимущественно гематогенной природы. Руководствуясь особенностями патогенеза гиалиноза сосудов, выделяют:
- простой сосудистый гиалин
Возникает вследствие инсудации неизмененных или малоизмененных компонентов плазмы крови, Такой тип гиалина чаще встречается у пациентов с доброкачественной гипертензией, атеросклерозе, а также у здоровых людей.
- липогиалин
Содержит липиды и бета-липопротеиды. Такой тип гиалина часто обнаруживается при сахарном диабете.
- сложный гиалин
Строится из иммунных комплексов, фибрина и разрушающихся структур сосудистой стенки. Такой гиалин характерен для пациентов с иммунопатологиями, например, с ревматическими заболеваниями.
Б) гиалиноз собственно соединительной ткани
Развивается, как правило, в исходе фибриноидного набухания, ведущего к деструкции коллагена и пропитыванию ткани белками плазмы и полисахаридами.
Имеет большое клиническое значение гиалиноз миометрия. После выполнения Кесарево сечения на матке остается рубец, на границе с мышцей в клетках откладывается гиалин. Если женщина будет рожать второго ребенка естественным путем, то произойдет разрыв.
Микроскопия: соединительнотканные пучки теряют фибриллярность, а клеточные элементы превращаются в хрящеподобную массу.
Гиалиноз может завершать фибриноидные изменения в очаге хронического воспаления. Гиалиноз как исход склероза имеет, в основном, местный характер: он развивается в рубцах, фиброзных спайках серозных полостей, сосудистой стенке при атеросклерозе.
Внешний вид: при выраженном гиалинозе внешний вид органов изменяется. Гиалиноз артериол и мелких артерий ведет к атрофии, деформации и сморщиванию органа. При гиалинозе собственно соединительной ткани она становится плотной, белесоватой, полупрозрачной.
Исход: в большинстве случаев неблагоприятный, однако, возможно и рассасывание гиалиновых масс.
4) Амилоидоз
Сопровождается глубоким нарушением белкового обмена, появлением аномального фибриллярного белка и образованием в межуточной ткани и стенках сосудов амилоида.
Амилоид представляет собой гликопротеид, основным компонентном которого являются фибриллярные белки (F-компонент, синтезируется амилоидобластами). Они образуют фибриллы. Фибриллярные белки амилоида неоднородны:
а) AA белок: неассоциированный с иммуноглобулинами, образующийся из своего сывороточного аналога – белка SAA
б) AL белок: ассоциированный с иммуноглобулинами, его предшественником являются легкие цепи иммуноглобулинов
в) AF белок: в его образовании участвует преальбумин
г) ASC1 белок – белок, предшественником которого также является преальбумин
Эти фибриллярные белки входят в сложные соединения с глюкопротеидами плазмы крови. Этот плазменный компонент (Р-компонент) амилоида представлен палочковидными структурами.
И F, и P-компоненты обладают антигенными свойствами. Фибриллы амилоида и плазменный компонент вступают в соединения в хондроитин-сульфатами ткани, а к образующемуся комплексу присоединяются «гематогенные добавки», среди которых основное значение имеют фибрин и иммунные комплексы. Все связи в амилоиде очень прочные, поэтому на него не действуют ферменты организма.
Классификация амилоидоза основывается на возможных причинах , специфике фибриллярных белков, распространенности, клинических проявлениях.
А. По причинам возникновения:
- первичный (идиопатический) амилоидоз
Для него характерно: отсутствие предшествующего или сопутствующего «причинного» заболевания; поражение преимущественно мезодермальных тканей – ССС, скелетных и гладких мышц, нервов и кожи; склонность к образованию узловатых отложений, непостоянство красочных реакций амилоидного вещества
- наследственный (генетический, семейный) амилоидоз
Наследственный амилоидоз с преимущественным поражением почек характерен для периодической болезни (семейная средиземноморская лихорадка), которая чаще наблюдается у представителей древних народов (евреи, армяне, арабы).
- вторичный (приобретенный) амилоидоз
В отличие от других форм развивается как осложнение, а не как самостоятельная болезни. К такому амилоидозу приводят хронические неспецифические воспалительные заболевания легких, туберкулез, остеомиелит, злокачественные новообразования, ревматические болезни.
Такой амилоидоз, как правило, генерализован и встречается наиболее часто.
- старческий амилоидоз
Типичны поражения сердца, артерий, головного мозга, островков Лангерганса. Эти изменения обуславливают физическую и психическую старческую деградацию. При старческом амилоидозе наиболее часты локальные формы, хотя встречается и генерализованный старческий амилоидоз.
Б. По специфике фибриллярных белков:
-AL-амилоидоз
Включает первичный (идиопатический) амилоидоз и амилоидоз при «плазмоклеточной дискразии», которая объединяет парапротеинемические лейкозы, злокачественные лимфомы и др.
Всегда генерализованный с поражением сердца, легких и сосудов.
-AA-амилоидоз
Охватывает вторичный амилоидоз и болезни Маккла и Уэльса. Также генерализован, но преимущественно поражает почки.
-AF-амилоидоз
Наследственный, представлен семейной амилоидной нефропатией. Поражаются, главным образом, периферические нервы.
-ASC1-амилоидоз
Старческий генерализованный или системный с преимущественным поражением сердца и сосудов.
В. По распространенности
-генерализованная форма
Первичный амилоидоз, амилоидоз при “плазмоклеточной дискразии” (AL), вторичный амилоидоз и некоторые типы наследственного (AA), старческий системный амилоидз (ASC1).
-локальный амилоидоз
Объединяет ряд форм наследственного и старческого амилоидоза, а также локальный опухолевидный амилоидоз.
Г. По клиническим проявлениям
-кардиопатический
Чаще встречается при первичном и старческом системном амилоидозе.
-нефропатический
При вторичном амилоидозе, периодической болезни и болезни Маккла и Уэллса.
-нейропатический
Как правило, имеет наследственный характер.
-гепатопатический
-эпинефропатический
-смешанный
Вторичный амилоидоз.
-APUD-амилоидоз
Развивается в органах APUD системы при развитии в них опухолей (апудом), а также в островках поджелудочной железы при старческом амилоидозе.
Морфо- и патогенез амилоидоза
Иногда функцию амилоидобластов выполняют макрофаги, плазматические клетки, фибробласты и т.д. При локальных формах в роли амилоидобластов могут выступать кардиомиоциты, гладкомышечные клетки, кератиноциты.
При вторичном амилоидозе (исключая амилоидоз при «плазмоклеточной дискразии») мутации и появление амилоидобластов можно связать длительной антигенной стимуляции.
Клеточные мутации при «плазмоклеточной дискразии» и при амилоидозе опухолей обусловлено опухолевыми мутагенами.
При генетическом амилоидозе речь идет о мутации гена, которая может произойти в различных локусах, чем и различаются составы амилоидных белков. Вероятно, имеют место подобные механизмы и при старческом амилоидозе.
Поскольку антигены белка амилоидных фибрилл являются чрезвычайно слабыми иммуногенами, мутирующие клетки не распознаются и не элиминируются. Развивается иммунологическая толерантность к белкам амилоида, что приводит к прогрессированию амилоидоза.
Образование амилоидного белка может быть связано с:
- ретикулярными волокнами (периретикулярный амилоидоз)
Амилоид выпадает по ходу мембран сосудов и желез, а также ретикулярной стромы паренхиматозных органов. Характерно преимущественное поражение селезенки, печени, почек, надпочечников, кишечника, интимы сосудов мелкого и среднего калибра (паренхиматозный амилоидоз).
-коллагеновыми волокнами (периколлагеновый)
Амилоид выпадает по ходу коллагеновых волокон, свойственно преимущественное поражение адвентиции сосудов среднего и крупного калибра, миокарда, поперечно-полосатой и гладкой мускулатуры, нервов, кожи (мезенхимальный амилоидоз).
Патогенез амилоидоза сложен и неоднозначен. Лучше всего изучен патогенез AA – и AL-амилоидоза.
При АА-амилоидозе фибриллы амилоида образуются из поступающего в макрофаг предшественника фибриллярного белка амилоида – белка SAA, который синтезируется в печени. Синтез SAA стимулирует макрофагальный медиатор интерлейкин-1, что приводит к резкому увеличению SAA в крови. В этих условиях макрофаги не осуществляют полную деградацию SAA, и из его фрагментов и инвагинатах плазматической мембраны амилоидобласта происходит сборка фибрилл амилоида. Эту сборку стимулирует амилоидстимулярующий фактор – АСФ, который обнаруживается в тканях в предамилоидной стадии.
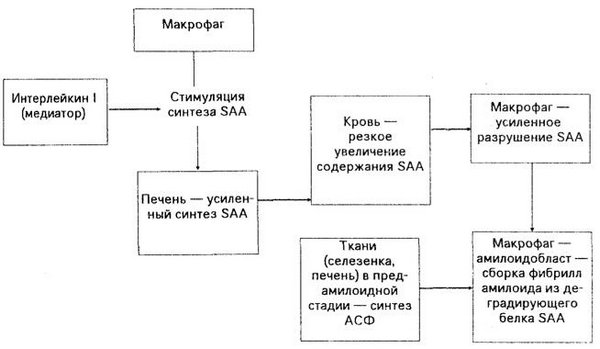
Итак, ведущую роль в патогенезе АА-амилоидоза играет магрофагальная система: она стимулирует усиленный синтез SAA,она же участвует в образовании фибрилл амилоида из деградирующих фрагментов белка.
При AL-амилоидозе сывороточным предшественником белка амилоидных фибрилл являются L-цепи иммуноглобулинов. Возможны два механизма образования AL-фибрилл: 1) нарушение деградации легких цепей с образованием фрагментов, способных к агрегации а фибриллы; 2) появление легких цепей с особыми вторичными и третичными структурами при аминокислотных заменах.
Синтез амилоидных фибрилл может происходить не только в макрофагах, но и в плазматических и миеломных клетках, синтезирующих парапротеины.
Соответственно, с извращенной функцией лимфоидной системы связано появление амилоидогенных легких цепей иммуноглобулинов – предшественника амилоидных фибрилл.

Макро- и микроскопия
Внешний вид органов зависит от степени процесса, Если отложения небольшие, внешний вид органа мало изменен. При выраженном амилоидозе орган увеличивается, становится очень плотным и ломким, а на разрезе имеет восковидный, сальный вид.
В селезенке амилоид откладывается в лимфатических фолликулах (саговая селезенка - плотная, увеличена, на разрезе полупрозрачные зерна) или равномерно по всей пульпе (сальная селезенка - увеличена, плотная, коричнево-красная, гладкая, имеет сальный блеск на разрезе).
В почках амилоид откладывается в стенке сосудов, в капиллярных петлях и мезангии клубочков, в базальных мембранах канальцев и в стреме. Почки становятся плотными, большими, сальными. По мере нарастания процесса клубочки и пирамиды полностью замещаются амилоидом, разрастается соединительная ткань и развивается амилоидное сморщивание.
В печени отложение амилоида наблюдается по ходу ретикулярной стромы долек. В стенках сосудов, протоков, соединительной ткани портальных трактов. Гепатоциты сморщиваются и погибают. Печень увеличена, плотная, выглядит сальной.
В кишечнике амилоид выпадает по ходу ретикулярной стромы слизистой, а также в стенках сосудов как слизистой оболочки, так и подслизистого слоя. При резко выраженном амилоидозе железистый аппарат кишечника атрофируется.
В сердце амилоид обнаруживается под эндокардом, в строме и сосудах миокарда, а также в эпикарде по ходу вен. Отложение ведет к амилоидной кардиомегалии. Сердце становится плотным, сальным.
Исход амилоидоза неблагоприятный.
2. Стромально-сосудистые липидозы
Возникают при нарушениях обмена нейтральных жиров или холестерина и его эфиров.
Нейтральные жиры – лабильные жиры, обеспечивающие энергетические запас организма.
Ожирение – увеличение количества нейтральных жиров в жировых депо, имеющее общий характер. Оно выражается в обильном отложении жиров в подкожной клетчатке, сальнике, брыжейке. средостении, эпикарде. Жировая ткань появляется также там, где она в норме отсутствует, например, в строме миокарда, поджелудочной железе.
Классификация основывается на различных принципах:
А. По этиологическому признаку:
-первичная форма
Его причина неизвестна, поэтому его называют идиопатическим.
-вторичная форма
Представлено следующими видами:
-алиментарное, причина которого – гиподинамия и несбалансированное питание
-церебральное, развивающееся при травме, опухолях, ряде нейротропных инфекций
-эндокринное-синдромы Иценко-Кушинга, Фрелиха
-наследственное – синдром Лоренса-Муна-Бидля, болезнь Гирке
Б. По внешним проявлениям:
-симметричный тип
Жиры откладываются равномерно в разных частях тела.
-верхний
Накопление в подкожной клетчатке лица, затылка, шеи, верхнего плечевого пояса, молочных желез.
-средний
Жир откладывается в подкожной клетчатке живота в виде фартука
-нижний
В области бедер и голеней
В. По превышению массы тела:
-I степень – 20-29% избыточной массы тела
-II степень – 30-49%
-III степень - 50-99%
-IV степень – 100% и более
Г. По характеристике морфологических изменений
Учитывают число адипоцитов и их размер.
-гипертрофический тип
Жировые клетки увеличены и содержат в несколько раз больше триглицеридов, чем обычные. Число адипоцитов не меняется. Адипоциты малочувствительны к инсулину, но высокочувствительны к липолитическим гормонам.
-гиперпластический тип
Число адипоцитов увеличивается. Функция адипоцитов не нарушена, метаболические изменения отсутствуют, течение болезни доброкачественное.
Причины и механизмы развития
Большое значение имеют несбалансированное питание, гиподинамия, нарушение ЦНС, эндокринной регуляции, наследственные факторы.
Непосредственный механизм ожирения лежит в нарушении равновесия липогенеза и липолиза в жировой клетке в пользу липогенеза.
Исход: редко бывает благоприятным.
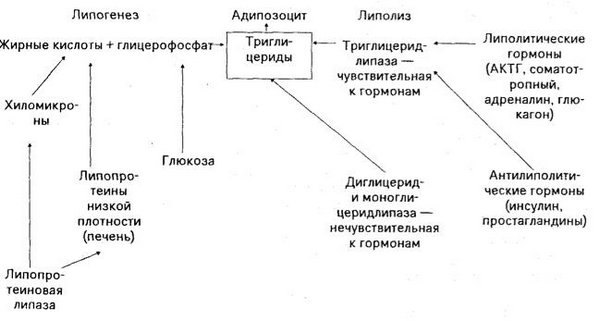
Нарушения обмена холестерина и его эфиров.
Такие нарушения лежат в основе атеросклероза. При этом в интиме артерий накапливаются и холестерин и его эфиры, но и бета-липопротеиды низкой плотности, и белки плазмы крови, чему способствует повышение сосудистой проницаемости.
Накопление ведет к деструкции интимы.
В результате в интиме образуется жиробелковый детрит, разрастается соединительная ткань, формируется фиброзная бляшка, сужающая просвет сосуда.
3. Стромально-сосудистые углеводные дистрофии
Могут быть связаны с нарушением баланса гликопротеидов и гликозаминогликанов.
Ослизнение тканей – дистрофия, связанная с нарушением обмена гликопротеидов. Хромотропные вещества высвобождаются из связей с белками и накапливаются в межуточном веществе. В отличие от мукоидного набухания при этом происходит замещение коллагеновых волокон слизеподобной массой. Соединительная ткань, строма органов, жировая ткань, хрящ становятся полупрозрачными, слизеподобными, а клетки их – звездчатыми.
Причина: чаще всего вследствие дисфункции эндокринных желе, истощения (например, микседема, слизистый отек, ослизнение соединительных тканей при кахексии).
Исход: процесс может быть обратимым, однако его прогрессирование приводит к колликвации и некрозу.


